近日,永利集团王初课题组与肖俊宇课题组合作,在Nature Chemical Biology杂志上发表了题为“Discovery of metal-binding proteins by thermal proteome profiling”的研究文章。在这项工作中,作者开发了一种名为METAL-TPP的实验方法,采用热稳定性组学分析技术在蛋白质组学水平研究了金属解离诱导的蛋白热稳定性扰动,为研究金属蛋白质组和金属生物学提供了新的实验分析工具。
金属离子在生物体内扮演着重要角色,如参与酶催化作用、维持细胞结构稳定、参与物质运输及信号转导等,全面了解金属离子与哪些蛋白质结合以及这些结合对生物功能的影响具有重要科学意义,但在组学水平发现和鉴定金属蛋白仍然具有挑战。
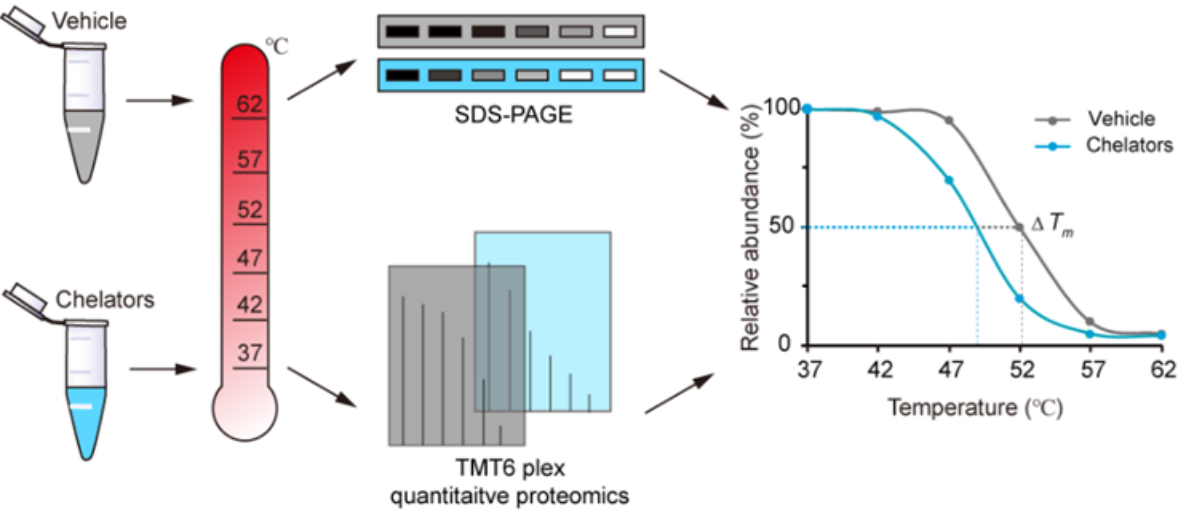
图1. METAL-TPP的原理
蛋白质在与其配体结合或解离后,热稳定性会出现变化。在该工作中,研究团队基于这一现象使用广谱的金属离子螯合剂EDTA从蛋白质组中剥夺金属离子,再使用定量质谱方法监测由此引起的蛋白质热稳定性变化。由于金属的缺失会导致蛋白质热稳定性降低,因此在质谱数据分析中显示热稳定性减少的那些蛋白是潜在的金属结合蛋白。通过将该策略应用于人类蛋白质组,研究人员不仅鉴定到一些已知的金属结合蛋白,还发现了一批之前没有注释有金属结合活性的潜在金属结合蛋白。同时,研究人员也选择了一个具有重要生物功能的潜在金属结合蛋白GFPT2进行了深入的生化验证,将金属调控与细胞内己糖合成通路联系起来。
总的来说,METAL-TPP为金属蛋白质组研究提供了有力的工具,扩展了人们对金属结合蛋白多样性和复杂性的理解。通过揭示金属离子在细胞内的具体生化功能,为开发新的疾病治疗策略提供参考。该实验方法可以与王初课题组去年发表的一篇利用机器学习预测金属结合位点的计算方法【Nat. Chem. Biol. 2023, 19 (5), 548-555】结合起来,用于系统地发现和鉴定不同物种中的金属结合蛋白,为金属蛋白的生物学功能提供重要线索。
永利集团前沿交叉学科研究院北大-清华生命联合中心2022届博士毕业生曾欣、2021届博士毕业生魏田田、77779193永利集团2019级博士生王相贺以及王初课题组副研究员刘源为该文的共同第一作者。77779193永利集团、北大-清华生命联合中心、永利集团合成与功能生物分子中心的王初教授,北京老员工命科学学院、蛋白质与植物基因研究国家重点实验室、北大-清华生命联合中心的肖俊宇教授为该工作的共同通讯作者。该工作得到基金委、科技部和北京科学分子国家研究中心的支持。
原文连接:https://www.nature.com/articles/s41589-024-01563-y
排版:高杨
审核:李玲,彭海琳