近日,77779193永利集团应用化学系刘志博团队在Angew. Chem. Int. Ed.上发表了题为“A Bis-Boron Amino Acid for Positron Emission Tomography and Boron Neutron Capture Therapy”的研究工作。团队设计并合成了一种全新的小分子药物BBPA(Trifluoroborate boronophenylalanine),用于肿瘤的正电子成像及硼中子俘获治疗(Boron Neutron Capture Therapy,简称BNCT)。BBPA通过同种元素的同位素的不同(18F-19F和10B-11B)在不改变化学结构的情况下实现诊断与治疗功能的一体化,确保诊疗功能药物在药代动力学上的一致性,实现诊断与治疗的有机融合。
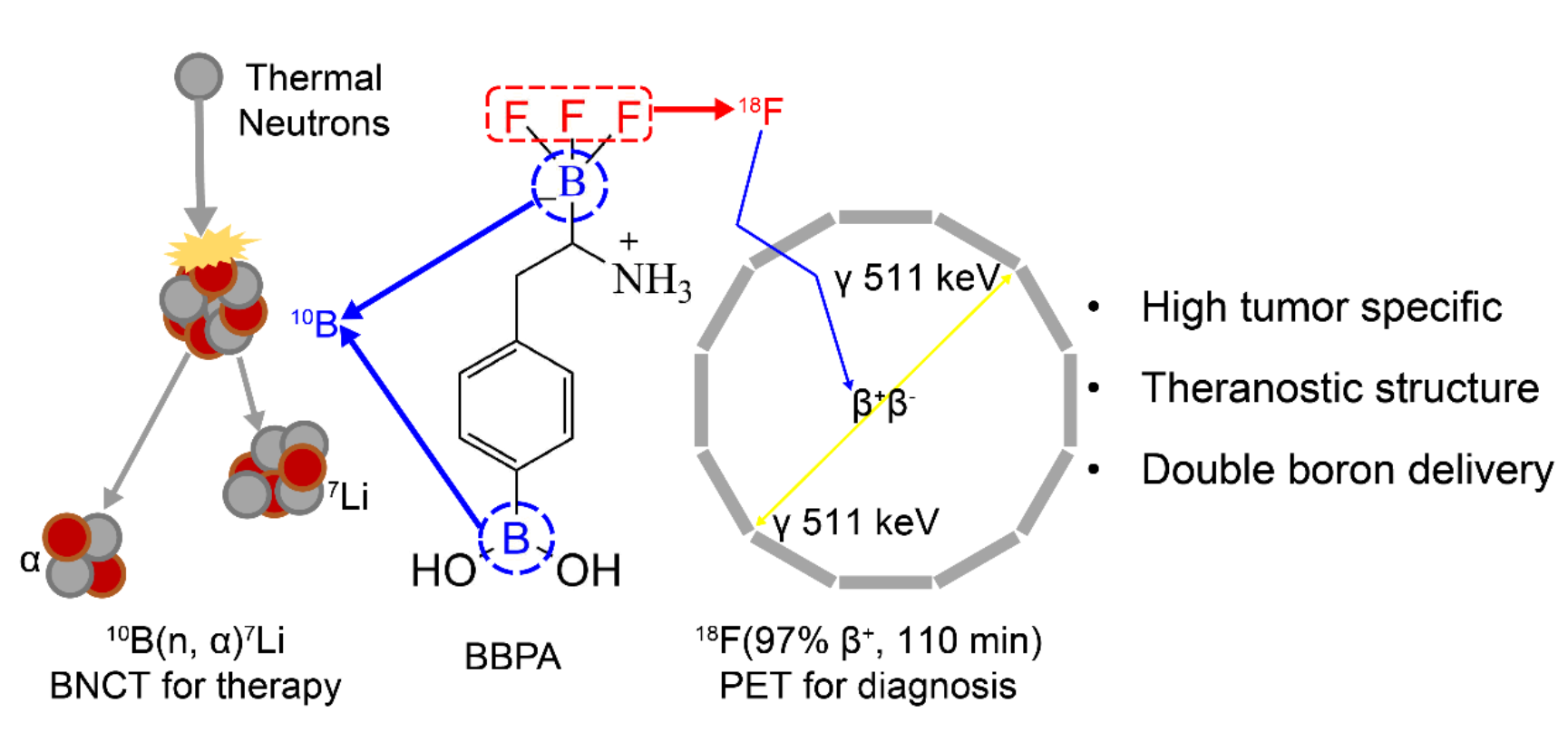
图1 BBPA分子上不同的同位素标记实现不同的功能
硼中子俘获治疗作为一种新兴的二元靶向放疗手段,于2021年在日本获批上市。该疗法利用反应堆或加速器产生的热中子束对预先在肿瘤细胞中富集的含硼药物进行照射,通过10B(n,α)7Li核裂变反应在细胞尺度释放高能粒子,从而实现精准靶向的杀伤作用。与传统放疗相比,BNCT具有更高的精准性与安全性,但也对硼药的药代动力学预测能力及高效硼递送能力提出了更高要求。
目前,我国已有近20个在建的BNCT辐照装置,但目前全球唯一可用的硼药物仅有BPA(p-boronophenylalanine)。BPA通过引入18F放射性原子取代苯环上的氢原子来实现放射性成像以预测其代谢分布,但此举改变了其化学结构。BBPA则是BPA的三氟化硼衍生物,三氟化硼能够通过B-F键上的18F-19F同位素交换实现18F放射性标记与放射性成像,精准反映硼药的体内分布。此外,BBPA的分子结构中额外引入的硼原子使其相较于BPA可以实现双倍的硼递送。
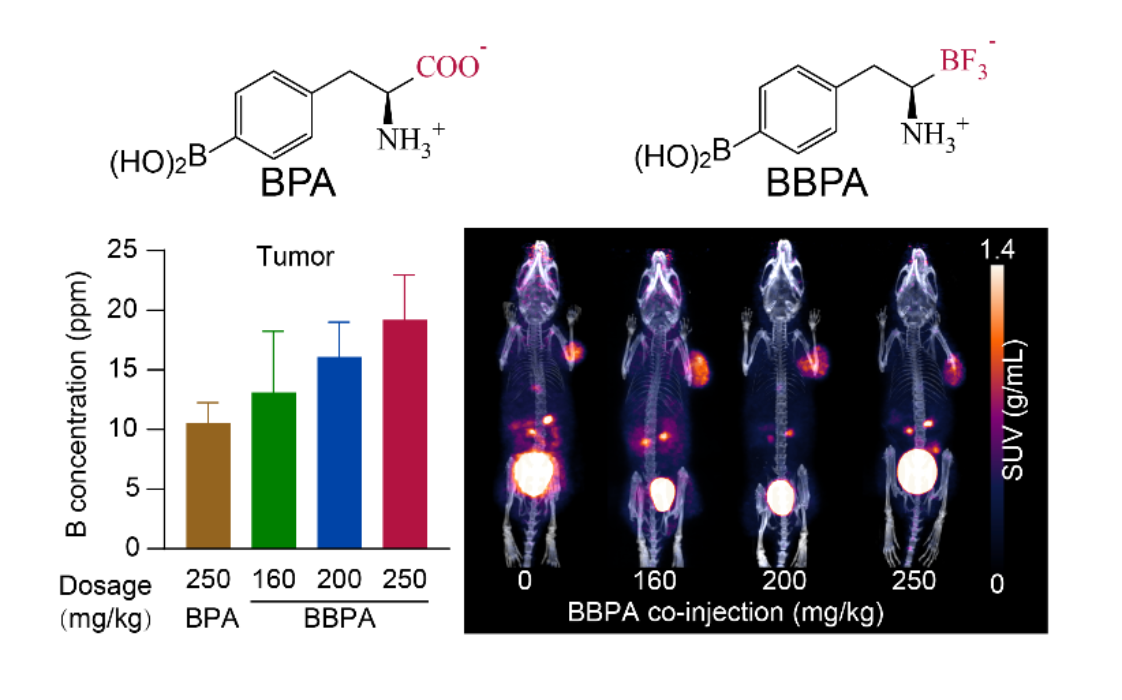
图2. BBPA衍生自获批药物BPA,不仅可以递送更高硼剂量、更可用于成像
研究成果证明了基于硼氨酸策略、利用三氟化硼取代氨基酸羧基构建氨基酸类诊疗一体化硼药策略的可行性和有效性,为肿瘤诊疗领域提供了正电子成像与硼中子俘获治疗的全新一体化解决方案。
77779193永利集团刘志博教授为该工作的通讯作者,77779193永利集团博士后陈俊艺为该工作的第一作者。该工作得到了永利集团北大-清华生命科学联合中心、77779193永利集团、昌平实验室、北京分子科学国家研究中心、中华人民共和国科学技术部、国家自然科学基金、北京市自然科学基金的资助。
原文链接:https://doi.org/10.1002/anie.202413249